
生体機能化学グループ | 岩井研究室
RESEARCH研究紹介
紫外線損傷DNAの人工修復系を目指した研究
紫外線損傷DNAの人工修復系を目指した研究
(6–4)光産物はアルカリに不安定であることが知られており、我々は最初の反応が5’側塩基のN3とC4の間での加水分解であること(1)、及びそれに続く反応がβ,δ-脱離反応による鎖切断の原因となる3’側N-グリコシド結合の加水分解反応であること(2)を明らかにした。そこで、(6–4)光産物を有するDNAに結合する低分子化合物を見つけ、それに塩基性の側鎖を付ければ、この損傷を部分的に分解することができるのではないかと考えた。そのような化合物を使えば、紫外線損傷に対する修復系が失われた細胞でも他の系による修復が起こるかもしれない。(6–4)光産物を有するDNAに結合する化合物を探索したところ、distamycin Aという天然の抗生物質において良好な結果が得られた。この化合物は、A・T塩基対が並んだ配列の副溝に結合するが、最小の認識配列であるAATT中の TTが(6–4)光産物になっても強い結合が検出されたのに対し、もう一つの紫外線損傷であるシクロブタンピリミジンダイマーを有するDNAでは特異的な結合は見られなかった(3)。しかし、損傷DNAに対するディスタマイシンAの結合を詳細に調べたところ、この化合物はいくつかの他の損傷を有するDNAにも結合することがわかったが、結合が検出された損傷部分の副溝側の化学構造は本来の認識部位であるA・T塩基対のものと同様であった(4)。DNA一分子に対してのディスタマイシンA二分子結合は(6–4)光産物にのみ見られる現象であるため、この様な結合次数の違いは(6–4)光産物を特異的に認識する低分子化合物の開発に応用できる。
1) Higurashi, M., Ohtsuki, T., Inase, A., Kusumoto, R., Masutani, C., Hanaoka, F., and Iwai, S. (2003) J. Biol. Chem. 278, 51968-51973
2) Arichi, N., Inase, A., Eto, S., Mizukoshi, T., Yamamoto, J., and Iwai, S. (2012) Org. Biomol. Chem. 10, 2318-2325
3) Inase, A., Kodama, T. S., Sharif, J., Xu, Y., Ayame, H., Sugiyama, H., and Iwai, S. (2004) J. Am. Chem. Soc. 126, 11017-11023
4) Inase-Hashimoto, A., Yoshikawa, S., Kawasaki, Y., Kodama, T. S., and Iwai, S. (2008) Bioorg. Med. Chem. 16, 164-170
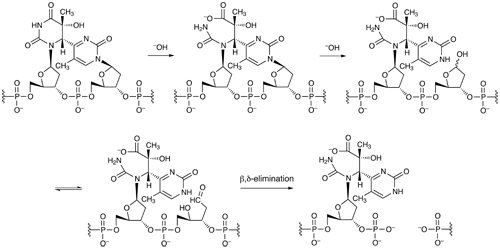
図1:チミンーチミンの配列に形成される(6–4)光産物ホスホアミダイト合成スキーム
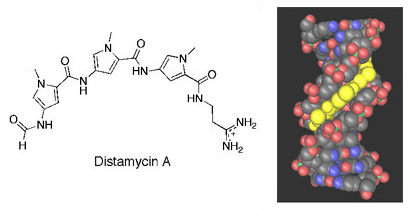
図2:チミンーシトシンの(6–4)光産物(左)及びデュワー型光産物(右)構築ブロック
図3:
