研究内容
現代の私たちの生活は有機化合物が無くしては成り立ちません。医薬品、繊維素材、プラスチック製品、光電子材料など、有機化合物はいろいろな形で身近な場所で使われています。このような有機化合物は、分子あるいはその集合体の構造によって多様な機能を発現するため、望みの機能や性質をもつ有機化合物を分子レベルで自在にかつ精密に合成する手法の開発は非常に重要です。
新谷研究室では、とくに
- 「触媒の力で有機分子の新たな反応性を引き出す」
ことを研究の中心に据え、
- 「新しい選択的有機合成反応の開発」
- 「新しい有機化合物の創成・機能開拓」
を柱とした次世代を切り拓く先端研究を通じて、物質科学の発展、さらには人類のより良い生活に貢献すべく研究に取り組んでいます。
1. 触媒金属の転位を活用した遠隔位不活性結合の活性化による新たな有機分子変換法の開拓
有機分子に普遍的に存在する炭素-水素結合をはじめとする安定で反応性の低い結合を触媒によって活性化し、新たな官能基導入や骨格構築へと導くことは、効率性に優れた新しい有機分子合成法の提供を可能にする有力かつ重要な研究です。当研究室ではとくに、反応活性点から遠隔位に存在し、通常では分子変換への利用が困難な不活性結合を活性化する手法として、遷移金属触媒を用いた反応において触媒金属の転位過程を利用する方法論の開拓を行っており、AIでは提案できないようなこれまでにない経路での高選択的有機合成反応の開発に取り組んでいます。
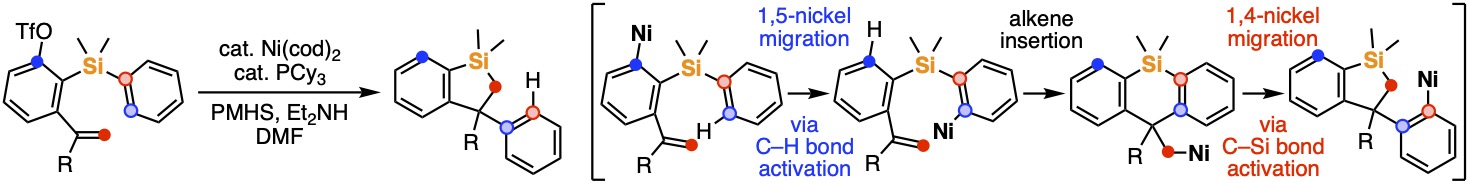
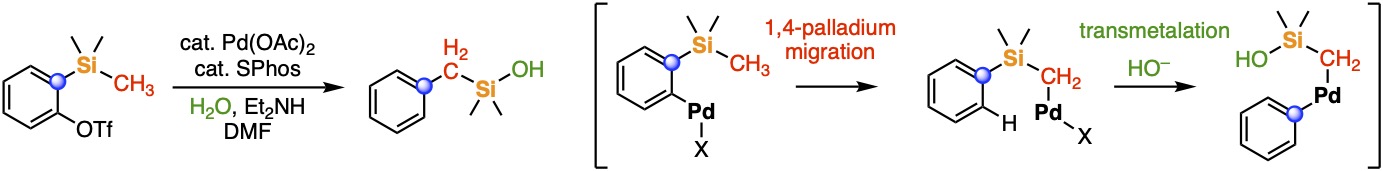
最近では、炭素の同族で類似性と相違性をあわせもつケイ素を含む有機分子の新規合成・活用に着目し、ニッケルやパラジウムを触媒金属とする炭素-水素ならびに炭素-ケイ素結合の新たな活性化法を見出しており、これにより従来法では合成困難な高い有用性が期待される含ケイ素有機化合物の新規合成法をいくつも開発しています[1]。例えば、ニッケルを用いた触媒系では、炭素-ニッケル結合と炭素-水素結合および炭素-ケイ素結合との交換反応を経由する新規連続プロセスによって、インダンのケイ素等価体である多置換シラインダンの選択的合成に成功しています[2]。また、パラジウム触媒を用いた炭素-水素結合および炭素-ケイ素結合の段階的な活性化により、アライン前駆体として知られる2-メチルシリルアリールトリフラートから位置選択的にベンジルシラノールを合成する新たな反応も見出しています[3]。
最近の発表論文
- 総説:Shintani, R. Chem. Lett. 2024, 53, upae132.
- Lee, D.; Fujii, I.; Shintani, R. ACS Catal. 2025, 15, 907.
- Shintani, R.; Tachibana, K. Angew. Chem., Int. Ed. 2026, 65, e2809429.
2. ケイ素求核剤を用いた新たな立体選択的有機合成反応の開発
ケイ素を含む有機化合物は、天然には存在しないが、有機合成における中間体としてばかりでなく、生理活性物質や機能性有機材料などとしても有用であり、注目を集めている化合物群です。しかしながら、従来の合成法ではアクセス可能な分子骨格が限られており、有機ケイ素化合物のさらなる機能開拓のためには新たな分子変換反応の開発が必要です。当研究室ではとくに、適切な触媒を用いて、不飽和結合をもつ有機分子にケイ素を求核剤として導入しながら複雑な有機ケイ素化合物を立体選択的に合成する手法の開発に取り組んでいます。
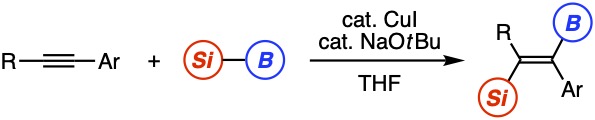
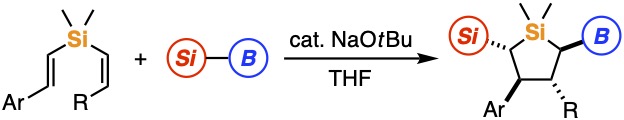
例えば、非対称な内部アルキンに対して、銅触媒存在下でシリルボロン酸エステルを反応させることにより、従来法では困難なアンチ付加でのシリルホウ素化が位置および立体選択的に進行し、対応するケイ素とホウ素を含む四置換アルケンの高選択的合成に成功しています[1,2]。また、調製容易なジアルケニルシランに対して、塩基触媒存在下でシリルボロン酸エステルを反応させると、環化を伴うシリルホウ素化が位置および立体選択的に進行し、対応するケイ素とホウ素を含む多置換シラシクロペンタンが高いジアステレオ選択性で得られることも見出しています[3]。
最近の発表論文
- Moniwa, H.; Shintani, R. Chem. Eur. J. 2021, 27, 7512.
- Moniwa, H.; Yamanaka, M.; Shintani, R. J. Am. Chem. Soc. 2023, 145, 23470.
- Ueji, K.; Shintani, R. Chem. Commun. 2026, 62, in press.
3. ラジカルの精密設計に基づく新たな有機分子変換法の開拓
ラジカルは高い反応性を示す重要な反応活性種であり、多様な有機分子変換に利用できることから、近年大きな注目を集めています。一方で、その高い反応性ゆえに選択性の制御は容易ではなく、これを実現するためにはラジカルの極性や立体環境を適切に設計することが重要です。
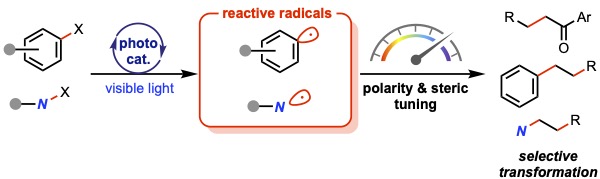
当研究室では、ラジカルの電子的・立体的性質を精密に変調することで、反応性と選択性を高度に制御する新たな有機分子変換法の開発に取り組んでいます。なかでも、可視光を駆動力とするフォトレドックス触媒反応は、このような精密制御されたラジカルを温和な条件で発生させることができる有力な手法です。とくに、アリールラジカルや窒素ラジカルをはじめとする各種ラジカル活性種に着目し、その性質を制御することで、従来法では達成が難しかった選択的分子変換への展開を目指しています。最近では、適切に設計したアリールラジカルをフォトレドックス触媒によって発生させることで、不活性な炭素-水素結合から選択的に水素原子を引抜き、それに続く炭素-炭素結合形成の実現に成功しており、ラジカルの電子的・立体的要因が反応性に大きく関与することを実験的・計算化学的に明らかにしています[1]。
最近の発表論文
- Fujii, I.; Mori, T.; Shintani, R. Tetrahedron 2026, 189, 134971.
4. 新規連鎖重合反応による新しい高分子合成
遷移金属錯体などの触媒を用いた有機合成反応は現代有機合成化学には不可欠なツールとして定着しており、高分子化合物の合成においても例外ではありません。用いる触媒によって特有の反応性を示すことが低分子化合物の精密有機合成において盛んに研究されており、これらの特徴を高分子合成へとうまく展開することができれば、既存の方法ではアクセス困難な新しい物性を発現しうる高分子化合物の効率的合成が可能になると考えられます。このような観点から当研究室では、触媒を用いた新しい形式による重合反応の開発による新規高分子化合物の創出に取り組んでいます。
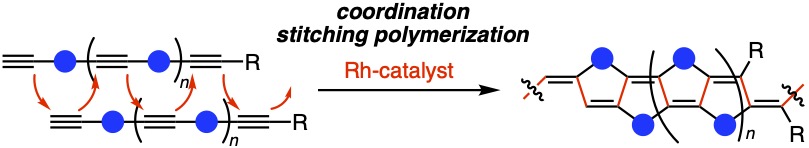
例えば、有機ロジウム種への炭素-炭素不飽和結合の挿入を経る触媒反応は強力な有機合成ツールの一つとして用いられており、これをベースに独自開発した「縫合反応」を用いた新しい重合プロセス「縫合重合」によって、従来法では合成できない新規π共役ポリマーの効率的合成およびその物性評価において成果を挙げています[1,2]。また、この縫合重合をアニオン重合やラジカル重合へと展開することにより、飽和型の縮環構造を繰返し単位にもつ耐熱性・透明性に優れた新規高分子の簡便かつ選択的な合成にも成功しています[3,4]。

最近の発表論文
- Ikeda, S.; Hanamura, Y.; Tada, H.; Shintani, R. J. Am. Chem. Soc. 2021, 143, 19559.
- Togawa, S.; Shintani, R. J. Am. Chem. Soc. 2022, 144, 18545.
- Ikeda, S.; Shintani, R. Chem. Commun. 2022, 58, 5281.
- Hamada, Y.; Togawa, S.; Shintani, R. J. Am. Chem. Soc. 2024, 146, 19310.
