- 日本語
- |
- English
有機合成化学グループ【 鷹谷研究室 】
| 教授 | 鷹谷 絢 |
|---|
新触媒・新反応で拓く次世代の物質合成化学
我々の生活は,多種多様な有機化合物に支えられて成り立っています(医薬・農薬、高分子材料、生体関連物質など)。“有機合成化学”とは,そのような有機化合物を自由自在に合成することができる唯一無二の学問であり,現代の人類社会の根幹を成す「分子レベルのモノづくり」といえるでしょう。物質科学・情報科学の発展に伴い,必要とされる物質の機能・構造がますます複雑化・多様化する一方で,資源問題や環境問題の顕在化によって,物質合成に課される制約(資源,エネルギー,廃棄物)はますます厳しくなっています。分子を創ることができる有機合成化学の役割は重要性を増しており,分子合成手法のさらなる革新が求められています。我々の研究グループでは,そのモノづくり技術革新の鍵となる「優れた機能を備えた遷移金属錯体触媒や反応活性種の創製」と「新しい分子変換反応の開発」を両輪とする有機合成化学研究を行っています。特に,多核金属錯体の構造と機能の精密制御に基づいた触媒開発や,有機典型元素や光エネルギーを利用した高反応性活性種の創製を基盤として,既存の方法では為し得ない革新的な分子変換反応の開発に取り組んでいます。ゼロからイチを創出する学術的基礎研究から,次世代の物質合成法開発の嚆矢となる新触媒・新反応を創出することを目指しています。
金属-金属結合の触媒機能の開拓
クロスカップリング反応を始めとする通常の金属触媒反応では,1つの金属原子が触媒として働きます。それに対して我々は,独自に開発した鋳型配位子を用いることで、金属-金属結合をもつ異種金属二核錯体の精密自在合成法を確立しました。これにより,周期表上の様々な2つの金属を組み合わせた新しい金属触媒ライブラリーが創出可能です。2つの金属が織りなす特異な電子状態・酸化状態,協働的な分子活性化・分子変換などを利用することで,従来の単核金属触媒では実現できなかった合成反応の開発や,従来触媒を凌駕する超高活性触媒の創出などを目指して研究を行っています。一例として,下図に示すような典型金属と遷移金属,あるいは2つの異なる遷移金属同士など,様々な組み合わせを持つ異種金属二核錯体の合成と構造解析に成功し,これらが二酸化炭素をはじめとする不活性分子の変換反応において優れた触媒活性を示すことを明らかとしました。我々の強みは,有機合成化学に基づいた“分子合成力”によって,多種多様な金属-金属結合を精密自在合成できる点にあります。独自の金属多核錯体ライブラリーを基に金属協働触媒の学理を確立し,新しい有機合成化学・金属触媒化学を開拓することを目指しています。
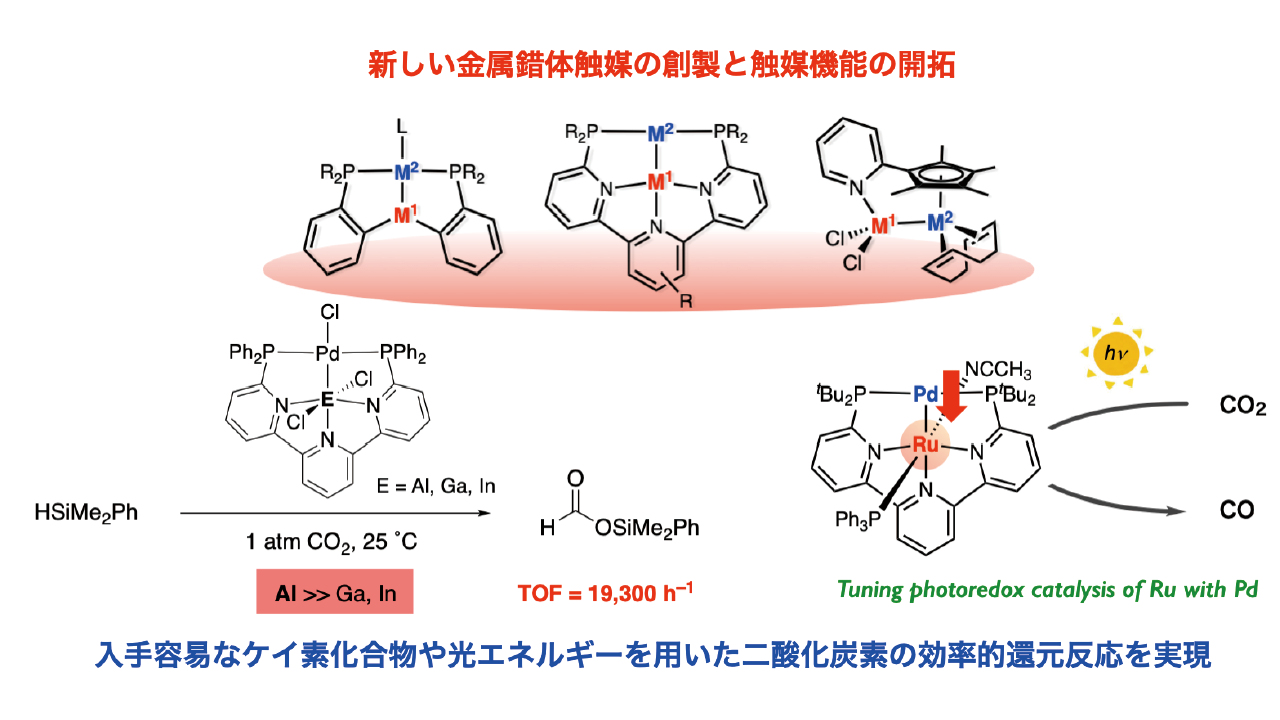
図1 金属-金属結合をもつ新触媒の創製と二酸化炭素の再資源化反応
光エネルギーを利用した安定結合・安定分子の変換反応の開発
有機分子の基本構造を成す炭素-炭素結合を直接的に切断し変換する反応は,従来の物質合成の常識を覆す革新的分子合成法として魅力的です。しかし,そのような反応を実現するには極めて高い反応性をもつ遷移金属錯体(特に希少な貴金属)や高温加熱条件などが必要とされます。我々は,光エネルギーと半金属元素や遷移金属元素を協働的に利用することで新しい高反応性活性種を創出し,希少な遷移金属元素に頼らない不活性結合変換反応や,高効率的かつ省資源型の革新的物質合成法の開発を目指した研究を行っています。一例として,ルイス塩基性のリン原子とルイス酸性のホウ素原子を併せ持つAmbiphilicホスフィン-ボラン化合物(Frustrated Lewis Pairs,FLPs)の効率的合成法の開発を基点とし,その光反応性の開拓に取り組んでいます。例えば,o-ホスフィノフェニルボラン誘導体に対して近紫外光を照射すると,リンからホウ素への1電子移動が進行することでビラジカル活性種(Frustrated Radical Pairs, FRPs)が発生し,ホウ素によるsp²炭素‒sp³炭素σ結合やベンゼン環炭素-炭素の切断反応が起こることを見出しました。さらに我々は,このビラジカル中間体(FRPs)を利用することで,光と熱を化学的刺激として用いるエチレンの可逆な捕捉・放出分子システムの開発にも成功しました。これにより,遷移金属を用いずにアルケンを捕捉・貯蔵したり,有用分子へ変換することが可能になります。
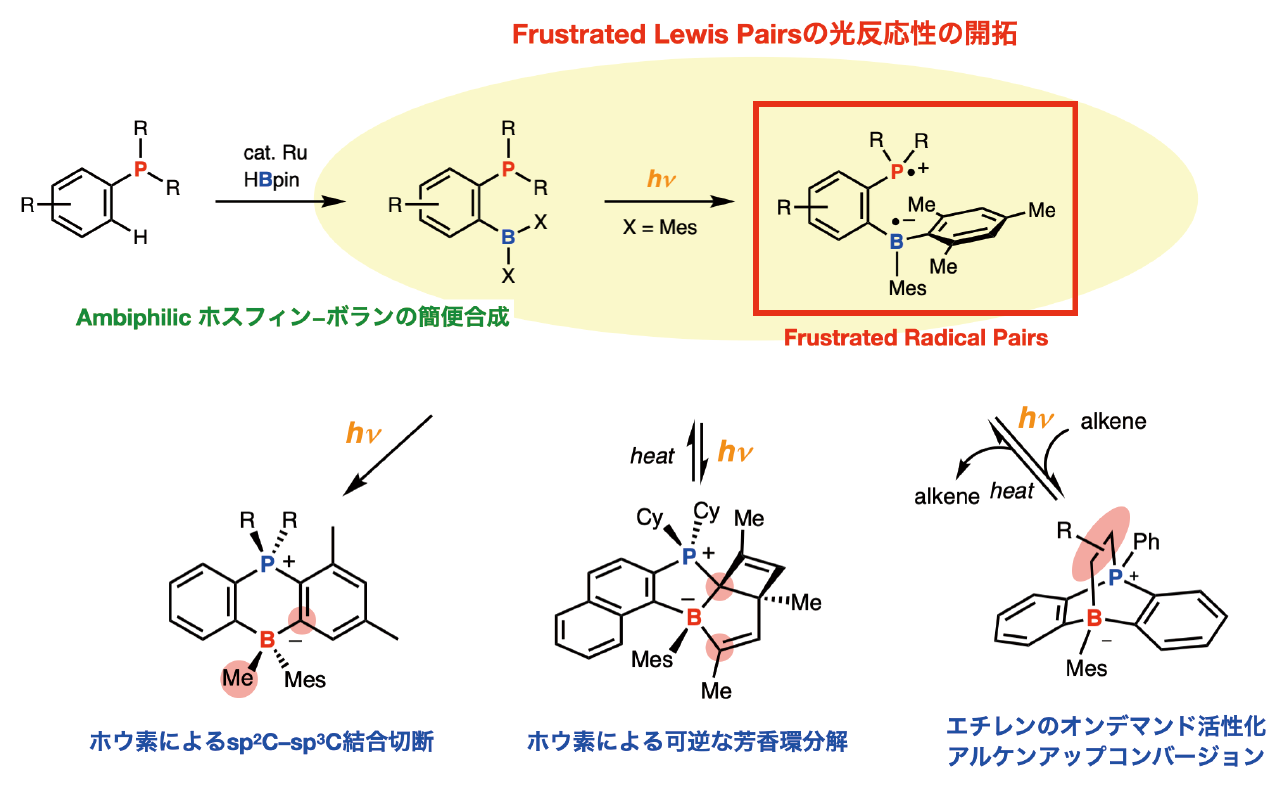
図2 ホウ素と光エネルギーの協働による革新的分子変換反応
また,様々なアリールケトン誘導体とピナコールボラン(HBpin)に対して,365 nmの光照射かつ加熱条件下でロジウム触媒を作用させると,アリールボロン酸エステルが良好な収率で得られることを見出しました。これは,単純ケトンのアシル基炭素-炭素σ結合を直接的に切断して分子間アリール化を実現した初の例です。また最近我々は,ピリジン(6員環)とシリルボランに対して近紫外~可視光を照射するとピロリジン誘導体(5員環)が得られるという新反応を発見しました。本反応は,ホウ素反応剤と光エネルギーによる活性化を利用することで,6員環芳香族化合物で あるピリジンから炭素原子1つを環外へと押し出し,5員環と3員環が縮環したピロリジン誘導体へと環構造を作り替えるものです。これにより,安価で大量に入手できるピリジンを原料として,医薬・農薬品として利用される高付加価値含窒素化合物を簡便に合成することが可能になります。これらのコンセプトに基づき,様々な“教科書に載っていない新反応”を開発中です。
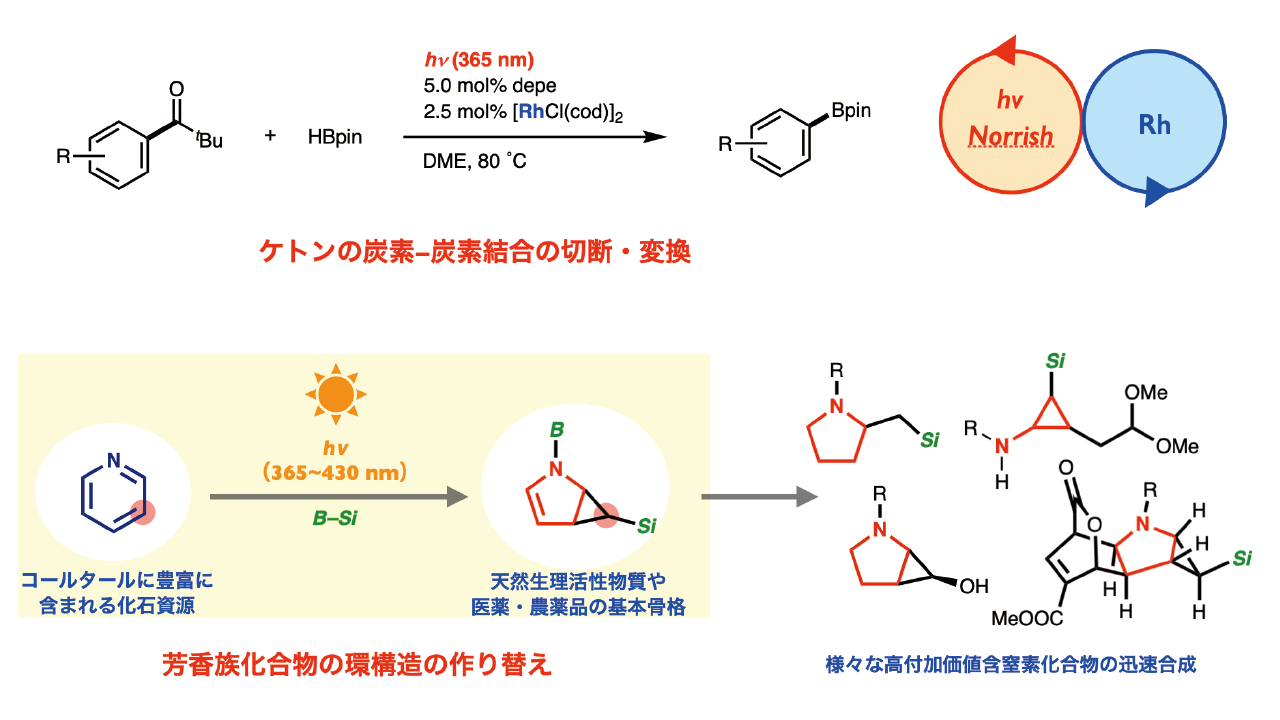
図3 光エネルギーを利用した炭素-炭素結合切断・芳香環分解反応